İyonik bağ
İyonik bağ, zıt yüklü iyonlar arasındaki elektrostatik kuvvetlere dayanan bir kimyasal bağ türüdür.
Oluşumu
En dıştaki yörüngeleri dolu olan atomlar oldukça kararlı durumdadırlar, başka atomlarla bileşik oluşturma eğilimi göstermezler. Sadece soygazların yörüngeleri tamamen doludur, diğer grupların dış kabuklarında eksik ya da fazla elektron bulunmaktadır.Oysa atom, tüm yörüngelerinin dolu olması yönelimindedir ve eğer dolu değilse bunu sağlamaya yönelecektir. Bu konumda atomun başına iki farklı olay gelebilir, dış kabuktaki elektronlardan kurtularak zaten dolu olan bir alttaki kabuğu son kabuk haline getirmek ya da dış kabuğu dışarıdan elektron alarak tamamlamak.
Elektron verme eğiliminde olan bir atomla elektron alma eğilimindeki bir atom reaksiyon alanına girdiklerinde, aralarında bir elektron alışverişi olur. Bunun sonucunda elektron alan atom negatif iyon (anyon), elektron veren atom ise pozitif iyon (katyon) haline gelecektir. Bu şekilde aralarında elektrostatik çekme kuvveti oluşan atomlar iyonik bağlı bir bileşik oluştururlar.
İyonik bağ oluşumunda, metal, düşük elektronegatifliği nedeniyle bir elektron vererek pozitif bir iyon (katyon) oluşturur. Normal sofra tuzunda, sodyum ile klor iyonları birbirlerine iyonik bağ ile bağlıdır. İyonik bağ genellikle metallerle ametaller arasında gerçekleşir. Ametal atomlarının elektronegatifliği yüksektir ve kolayca elektron alıp negatif iyon (anyon) oluşturabilirler. Dolayısıyla, iki veya daha fazla iyon, elektrostatik kuvvetlerin etkisiyle birbirlerini çekerler. Bu tür bağlar, hidrojen bağından daha kuvvetli fakat kovalent bağ ile hemen hemen aynı kuvvettedir.
Özellikleri
- Katı halde genellikle elektriği iletmezler fakat sulu çözeltilerinde ve erimiş halde iyonlarına ayrıştıkları için elektrik akımını iletirler.
- Sert ve kırılgandırlar, tel ve levha haline getirilemezler, herhangi bir zorlamada kırılırlar.
- İyonik bileşiklerin formülünü yazarken katyon başa gelir.
- Elektroliz edilebilirler
- İyonik bileşikler oda sıcaklığında genellikle katı halde ve kristal yapıda bulunur.[1]
İyonik bağlanma yalnızca, bağlanmış atomlar serbest olanlardan daha düşük enerjiye sahip olduklarında ve reaksiyonun toplam enerji değişimi, reaksiyonun gerçekleşmesi yönünde ise meydana gelir. Toplam enerji değişimi ne kadar büyükse, bağ o kadar güçlüdür. Tüm iyonik bağlar bir tür kovalent ya da metalik bağ özelliği taşırlar. İki atom arasındaki elektronegatiflik farkı ne kadar büyükse bağ da o kadar iyoniktir.
Sağlamlığı
İyonik bağın sağlamlığı iki şeye bağlıdır:
- İyonların yüklerinin çarpımının mutlak değerine,
- İyon yarıçapına
Çünkü Coulomb yasasına göre çekim kuvveti yüklerin büyüklüğüyle doğru orantılı, yükler arası uzaklığın karesiyle ters orantılıdır. İyonik bağın sağlamlığı bileşiğin erime noktasına bakılarak anlaşılabilir. Erime noktası yüksek olan bileşiklerin iyonik bağı da kuvvetlidir.
Örneğin Ca2+ ve Ba2+ iyonları O2- ile iyonik bağ yapınca yükler eşit olmasına rağmen Ca2+ nun iyon yarıçapı daha küçük olduğundan CaO daha sağlamdır ve erime noktası daha yüksektir, yandaki tabloda da görülebilir.
| Bileşik | Erime noktası (°C) |
|---|---|
| NaF | 993 |
| NaCl | 801 |
| NaBr | 750 |
| NaI | 662 |
| KCl | 772 |
| KBr | 735 |
| KI | 680 |
| BaO | 1918 |
| CaO | 2614 |
| MgCl2 | 714 |
| MgO | 2852 |
Kutuplaşma (polarizasyon) etkisi
İyonik bileşiklerin kristal yapısı içindeki iyonlar küreseldir fakat eğer artı iyon küçük ve/veya yüksek oranda yüklüyse, eksi iyonun elektron bulutunu bozar. Eksi iyonun bu şekilde kutuplaşması, iki atomun çekirdekleri arasında ilave yük birikimine yol açar ki bu da kısmi kovalent bağ demektir. Boyutça büyük eksi iyonlar daha kolaylıkla polarize olurlar. Fakat bu durum, yalnızca 3+ değerlikli artı iyon (örneğin, Al3+) söz konusu olduğunda önemlidir (örneğin, saf AlCl3 kovalent bir moleküldür). Öte yandan, 2+ yüklü iyonlar (Be2+) hatta 1+ yüklü iyonlar (Li+) dahi, boyutları çok küçük olduğu için bir miktar kutuplaştırma (polarize etme) gücüne sahiptirler (örneğin, LiI iyoniktir fakat bazı kovalent özellikler gösterir). "Kutuplaştırma gücü", iyonun yükü ile boyutu arasındaki orana bağlı olup yük yoğunluğu olarak adlandırılır.
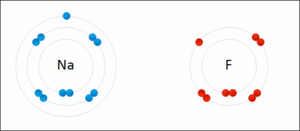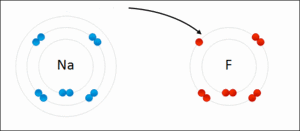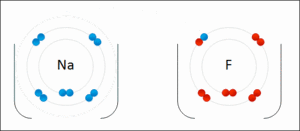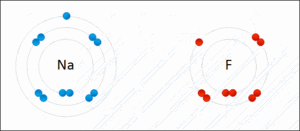
Sodyum ve klor atomlarının sodyum klorid oluşturmak üzere iyonik bağla bağlanışı. Sodyum en dıştaki atomunu kaybeder ve asal gaz elektron konfigürasyonuna sahip olur. Bu elektron egzotermik olarak klor atomuna girer. Ardından, zıt yüklü iyonlar birbirini çeker ve iyonik bağ oluşur.
Klor atomunun, sodyum atomunun son katmanındaki bir elektronu alarak negatif yükle yüklenir. Böylece klor anyonu oluşur.Sodyum atomu ise bir elektonu eksildiği için pozitif yükle yüklenerek sodyum katyonunu oluşturur. Oluşan anyon ve katyon zıt yüklere sahip oldukları için birbirini çeker. Anyon ve katyon arasındaki bu çekim kuvvetli bir kimyasal bağdır ve bu kimyasal bağ iyonik bağ olarak adlandırılır.
Kovalent bileşiklerle karşılaştırılması
İyonik bir bağ durumunda atomlar, zıt yüklü iyonların çekimi ile birbirine bağlı iken, kovalent bağ durumunda atomlar, elektron paylaşımı yoluyla bağlanırlar. Kovalent bağ durumunda, her atomun etrafındaki moleküler geometri, VSEPR kuralları[3] ile belirlenirken, iyonik malzemelerde geometri, maksimum sıkıpaket kurallarını takip eder. Dolayısıyla bir bileşiğin iyonik ya da kovalent olarak sınıflandırılması vardır.
Ayrıca bakınız
Kaynakça
- ↑ İyonik Bağlar Buyutec.net 26 Haziran 2015. Erişim tarihi: 26 Haziran 2015.
- ↑ MEB (2012). 10.Sınıf Kimya Ders Kitabı. s. 144-146. http://www.meb.gov.tr/Ders_Kitaplari/2012/OrtaOgretim/Devlet/OrtaOgrt/Kimya_10.pdf. Erişim tarihi: Şubat 19, 2013.
- ↑ VSEPR = Valence Shell Electron Pair Repulsion theory (Valans kabuğu elektron çifti itme teorisi) (1957): Kimya'da bir model olup bireysel moleküllerin şekillerini tanımlamayı hedefler.