Polar bağ
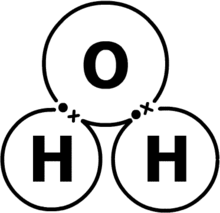
H2O Polar bağ örneği
Polar bağ, farklı tür atomların bir araya gelerek vektörel olarak net kuvvetin sıfırdan farklı olduğu bağ türüdür. Karbondioksit, su, metan vb farklı atomlar içeren kovalent bağlı bileşikler örnek verilebilir. Bağların gücü karşılaştırılırsa ya polar bağın gücü apolar bağın gücüne eşit ya da polar bağ daha güçlüdür. Bunun nedeni son katmanlarındaki elektron sayısı farkıdır. Elektron sayısı farkı ne kadar büyükse bağda o kadar güçlü olur.
Polar bağ da bir negatif bir de pozitif uç bulunur. H2O polar bağ örneğinde Hidrojen tek elektrona sahip olduğu için bağ yapamaz. Bu sebep ile Oksijenin bir elektronunu ortak kullanarak bağ yapmış olur.[1]
Kaynakça
- ↑ Polar Kovalent Bağ Buyutec.net 26 Haziran 2015. Erişim tarihi: 26 Haziran 2015.
This article is issued from Vikipedi - version of the 5/26/2016. The text is available under the Creative Commons Attribution/Share Alike but additional terms may apply for the media files.