Alüminyum klorür
| Alüminyum klorür | |
|---|---|
 | |
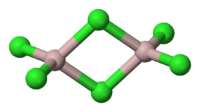 | |
| aluminium chloride | |
| Diğer adlar aluminium(III) chloride aluminum trichloride | |
| Tanımlayıcılar | |
| CAS numarası | 7446-70-0, 10124-27-3 |
| PubChem | 24012 |
| EC numarası | 215-481-4 |
| ChEBI | CHEBI:30114 |
| RTECS numarası | BD0530000 |
| ATC kodu | L01 |
| SMILES |
|
| InChI |
|
| ChemSpider | 22445 |
| Özellikler | |
| Molekül formülü | AlCl3 |
| Molar kütle | 133.34 g/mol (anhydrous) 241.43 g/mol (hexahydrate) |
| Görünüm | beyaz veya açık sarı katı, hygroscopic |
| Yoğunluk | 2.48 g/cm3 (anhydrous) 1.3 g/cm3 (hexahydrate) |
| Erime noktası |
192.4 ( |
| Kaynama noktası |
120 |
| Çözünürlük (su içinde) | 43.9 g/100 ml (0 °C) 44.9 g/100 ml (10 °C) 45.8 g/100 ml (20 °C) 46.6 g/100 ml (30 °C) 47.3 g/100 ml (40 °C) 48.1 g/100 ml (60 °C) 48.6 g/100 ml (80 °C) 49 g/100 ml (100 °C) |
| Tehlikeler | |
| R-ibareleri | R34 |
| NFPA 704 |
 0
3
2
|
| LD50 | 380 mg/kg, rat (oral) hexahydrate: 3311 mg/kg, rat (oral) |
| Belirtilmiş yerler dışında verilmiş olan veriler, standart haldedir. (25 °C, 100 kPa) | |
| Bilgikutusu kaynakları | |
Alüminyum klorür (AlCl3), alüminyum ve klorürün temel bileşiği. Rengi genel olarak beyazdır fakat Demir(III) klorür ile etkileşime girdiğinde sarı bir renk alır. Katı erime ve kaynama noktası düşüktür. Genel olarak alüminyum metallerin üretiminde kullanılır. Ayrıca kimya endüstrisinin diğer alanlarında da yüksek miktarda kullanılır. Bileşik sıklıkla Lewis asiti olarak anılır.
Yapısı
Susuz
AlCl3 üç farklı yapıda bulunur, dereceye ve duruma göre (Katı, sıvı, gaz). Katı AlCl3, tabaka katmanlı kübik paketlenmiş tabakalar halindedir. Bu çerçevede, Al Oktahedral koordinasyon geometrisi şeklindedir.[1]
Heksahidrat
Heksahidarat[Al(H2O)6]3+ merkezler ve klorür karşı iyonlarından oluşur. Hidrojen bağı katyon ve anyonları birbirine bağlar.[2]
Kaynakça
- ↑ Bunun tersine, AlBr3 daha moleküler bir yapıdadır. Al3+ ile birlikte iyonların komşu paket çercevelerinin tetrahedral deliklerini işgal eder durumdadır. Br− ions.A. F. Wells, Structural Inorganic Chemistry, Oxford Press, Oxford, United Kingdom, 1984.
- ↑ Andress, K.R.; Carpenter, C. "Kristallhydrate. II.Die Struktur von Chromchlorid- und Aluminiumchloridhexahydrat" Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie 1934, volume 87, p446-p463.
Dış bağlantılar
- International Chemical Safety Card 1125
- Index of Organic Synthesis procedures that utilize AlCl3
- The period 3 chlorides
- MSDS
- Government of Canada Fact Sheets and Frequently Asked Questions: Aluminum Salts
| ||||||||||||||||||||