Serin
| Serin | |
|---|---|
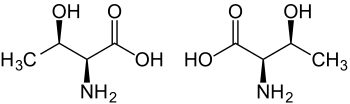 | |
| Serin L-Serin (sol) DSerin (sağ) | |
| Tanımlayıcılar | |
| CAS numarası | 302-84-1 |
| PubChem | 617 |
| EC-numarası | 206-130-6 |
| SMILES |
|
| InChI |
|
| ChemSpider | 5736 |
| Özellikler | |
| Molekül formülü | C4H9NO3 |
| Molar kütle | 105,09 g·mol−1 |
| Görünüm | Katı,beyaz, iğne şeklindeki kristal görünüöü ve tatlı. |
| Erime noktası |
215–225 °C |
| Çözünürlük (su içinde) | Suda iyi çözülür (360 g·l−1 bei 20 °C). Dietileter'de çözülmez |
| Tehlikeler | |
| AB İndeksi | Belirtilmemiş |
| Belirtilmiş yerler dışında verilmiş olan veriler, standart haldedir. (25 °C, 100 kPa) | |
| Bilgikutusu kaynakları | |
Serin (Ser, S), organik bir molekül ve aynı zamanda hayvansal proteinlerde sıkça bulunan aminoasitlerden biridir. Hayvansal proteinlerde serinin sadece L-stereoizomeri bulunur. Serin insan vücudu tarafından glisin gibi diğer metabolitlerden sentezlenebildiği için dışarıdan beslenme yoluyla alınması şart değildir. Serin, ilk olarak ipek proteinlerinden 1865 yılında izole edilmiştir. İpek bol miktarda serin içerir. Serin ismini, ipek'in latincesi sericum 'dan almaktadır. Serin'in moleküler yapısı ilk defa 1902 yılında çözülmüştür.
Bu yazıda ya da bilimsel makalelerde Serin L- ya da D- olarak hiçbir ön ek almayarak sadece Serin diye bahsedilmişse, burda bahsi geçen L-Serin’dir.
Sentezi
Serin ve glisinin sentezi 3-fosfogliserat'ın oksidasyonuyla başlar. Bu oksidasyon reaksiyonundan elde edilen 3-fosfohidroksipirüvat, glutamik asitle bir transaminasyon reaksiyonunda kullanılır. Bu tepkimenin sonucunda üretilen 3-fosfoserin'den inorganik fosfat (Pi) grubunun ayrılması sonucunda serin sentezi tamamlanmış olur.
Fonksiyonları
Serinin metabolizmada önemli fonksiyonları vardır. Pürinler, pirimidinler, sistein, triptofan (bakterilerde) ve daha birçok metabolitin biyosentezinde serin önemli bir role sahiptir.
Enzimlerin moleküler yapısına dahil edildiğinde, serinin, katalitik fonksiyonların yerine getirilmesinde çok önemli rolleri bulunur. Kemotripsin ve tripsin gibi birçok enzimin katalitik olarak aktif olan kısımlarında serin bulunduğu gözlenmiştir. Sinir gazları ve haşere ilaçlarında kullanılan bazı kimyasal maddeler, asetilkolin esteraz enziminin katalitik aktif bölgesindeki serin molekülünü kimyasal olarak değiştirerek bu enzimin fizyolojik fonksiyonunu tamamiyle engellerler. Esteraz enziminin enzimatik aktivitesinin yokluğunda, asetilkolin isimli nörotransmitter kısa süre içerisinde organizma için hayati tehlike oluşturacak bir ölçüde birikir, kasılmalar ve ölüm vuku bulur.
Serin racemerase enzimi tarafından substrat olarak L-serin kullanılarak sentezlenen D-serin, sinir hücrelerinin iletişiminde kullanılan bir moleküldür.
Kaynakça
- ↑ Hans-Dieter Jakubke, Hans Jeschkeit: Aminosäuren, Peptide, Proteine, Verlag Chemie, Weinheim, S. 470, 1982, ISBN 3-527-25892-2.
| ||||||